|
||||
|
|
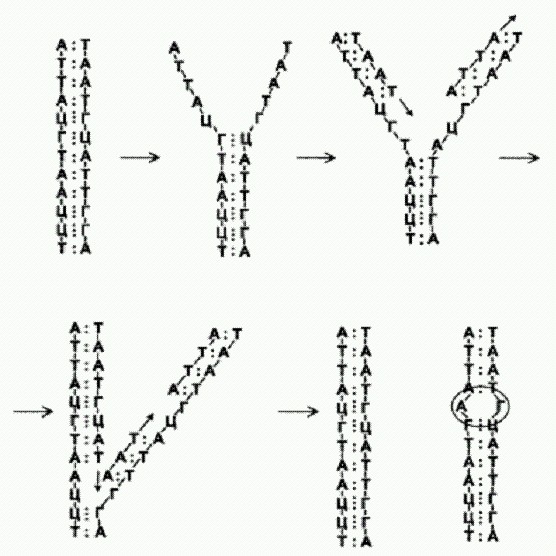
ГЛАВА 7. УПРАВЛЯЕМЫЕ МУТАЦИИВеликие открытия 50-60-х годов XX века, такие как расшифровка структуры ДНК и генетического кода, произвели столь сильное впечатление на научное сообщество, что наспех оформившиеся вокруг этих открытий теории сразу же стали считаться "классическими". Дальнейшее развитие биологии показало, что не стоило так торопиться. Что ж, зато с тех пор молекулярные биологи не могут пожаловаться на недостаток сенсационности в своих открытиях. Стоит ученым обнаружить какой-нибудь новый молекулярный механизм, глядишь, одна-две "догмы" сразу же и рушатся. И тотчас падкие на сенсации журналисты привычной рукой строчат броские заголовки: "Теория эволюции под вопросом" и "Дарвин опровергнут". Хотя уж кто-кто, а Дарвин тут точно ни при чем. И факт эволюции никто из серьезных ученых под сомнение не ставит. Просто нужно честно признать, что в работе молекулярных систем, отвечающих за обработку генетической информации, очень много неизвестного и непонятного. И каждое новое открытие приближает нас к пониманию того, как на самом деле идет эволюция на молекулярном уровне. Пожалуй, из всех скороспелых "абсолютных истин" синтетической теории эволюции с самым громким треском рухнула догма о полной случайности всех наследственных изменений. Произошло это лишь в последние 10-20 лет, и многие биологи даже не успели еще вполне осознать этот факт. До сих пор и в популярных текстах, и даже в учебниках и научных статьях продолжают встречаться ссылки на "случайность всех мутаций" как на что-то общеизвестное и не подлежащее сомнению. Однако на сегодняшний день твердо установлено, что живая клетка располагает большим арсеналом средств, позволяющих ей контролировать изменения своего генома. Вообще-то этого следовало ожидать. Ведь мутации — изменения нуклеотидной последовательности ДНК — являются важным фактором, влияющим на жизнеспособность организмов. И это влияние проявляется не когда-то в отдаленном будущем, а здесь и сейчас — у самого организма или его непосредственных потомков. Если организмы в ходе эволюции могут выработать приспособления, например, для защиты от хищников или болезнетворных микробов или для контроля температуры тела, то почему они не имеют права выработать также и приспособления, позволяющие им контролировать мутации? Никакого теоретического запрета на такие приспособления вроде бы нет, однако биологи-теоретики почему-то довольно долго считали их запрещенными. Наверное, дело тут в том, что в большинстве ситуаций единственное, чего хочет добиться организм от мутационного процесса, — это чтобы он шел как можно медленнее или не шел вовсе. В стабильных благоприятных условиях это вполне разумно. Зачем менять свою наследственность, если все и так хорошо? Однако сама жизнь не позволяет долго существовать, совершенно не меняясь. Не идти вперед — значит идти назад. Для начала вспомним, чему нас учили в школе на уроках биологии. Главный источник мутаций — ошибки, возникающие в ходе копирования ДНК. ДНК в норме состоит из двух комплементарных цепочек нуклеотидов. Нуклеотид А всегда стоит напротив Т, Г — напротив Ц. Пары Г-Ц более прочные, они удерживаются вместе тремя водородными связями, а пары А-Т — только двумя.
Во время репликации (копирования, удвоения) две цепочки разделяются, и на каждой по принципу комплементарности синтезируется новая цепочка, как показано на рисунке. Синтез осуществляется при помощи фермента ДНК-зависимой ДНК- полимеразы. Одна из двух новых цепей синтезируется подряд, без перерывов, потому что направление ее синтеза совпадает с направлением "расплетания" двойной спирали исходной молекулы ДНК. Вторая цепь синтезируется кусочками, задом наперед. Эти кусочки называются "фрагментами Оказаки" (в честь их первооткрывателя, японского молекулярного биолога Редзи Оказаки, пережившего бомбардировку Хиросимы и скончавшегося в 1975 году в 45-летнем возрасте от лейкемии). В итоге получаются две одинаковые молекулы, каждая из двух комплементарных цепей. На приведенном рисунке возникла мутация — в правой молекуле напротив одного из гуанинов (Г) случайно встал аденин (А) вместо цитозина (Ц). Скорее всего, эта мутация будет замечена и исправлена специальными ферментами, функция которых как раз и состоит в исправлении подобных ошибок. Починку "неправильных" или поврежденных участков ДНК называют репарацией. В нашем примере мутация возникла случайно. Впрочем, постойте. Случайно ли? Она ведь возникла на стыке двух фрагментов Оказаки, а процесс соединения этих фрагментов — некая особая операция, "технологически" отличающаяся от других этапов репликации, расплетания спирали и присоединения комплементарных нуклеотидов. Может быть, в нашей клетке забарахлила система соединения фрагментов Оказаки? А может, она забарахлила не случайно, а потому, что на нее оказал воздействие какой-то внешний или внутренний фактор? А если он внутренний, то клетка, наверное, может как-то контролировать его? А тогда, если хорошенько разобраться, не может ли в конечном счете оказаться так, что сама клетка "отдала команду" осуществить мутацию в данном месте ДНК? Если мы всерьез задумаемся над этими вопросами, то поймем, что было бы крайне удивительно, если бы живая клетка за 4 миллиарда лет эволюции так и не выработала никаких механизмов управления мутационным процессом. Ведь такие механизмы, во-первых, вполне возможны, во-вторых, могли бы оказаться очень полезными. Впрочем, нет повода сомневаться в том, что значительная часть мутаций действительно возникает случайно — просто потому, что никакое копировальное устройство не может работать с абсолютной точностью. Кроме того, мутации могут происходить и без репликации, пока ДНК находится в двухцепочечном состоянии, — например, нуклеотиды могут претерпевать химические изменения под воздействием радиации, ультрафиолета или свободных радикалов, возникающих в ходе клеточного дыхания. Большинство ошибок в цепях ДНК будет замечено и исправлено, но какую-то небольшую их часть пропустит, не заметит даже самый строгий молекулярный "корректор". Но мутации возникают не только потому, что невозможно копировать ДНК с абсолютной точностью. Мы привыкли думать, что мутации — это всегда некое нарушение, неправильность, ошибка, то есть что-то нежелательное, "мешающее нормально жить". В действительности это не всегда так. Изменение наследственной информации — неотъемлемая и необходимая часть жизни. Если бы геномы не менялись, на нашей планете, возможно, до сих пор жил бы только один вид очень примитивных микробов — тот самый Лука, общий предок всего живого (см. главу "Происхождение жизни"). Впрочем, и он бы давно вымер, не смог бы долго продержаться с неизменным геномом. А если бы молекулы РНК копировались с абсолютной точностью на этапе "преджизни", то и никакой Лука никогда бы не появился. Об этом, между прочим, свидетельствуют результаты экспериментов, проводимых исследователями РНК-мира. Для того чтобы в сообществе размножающихся молекул РНК зародилось что-то новое и полезное, совершенно необходимо, чтобы отдельные короткие молекулы, соединяясь в более длинные, могли обмениваться друг с другом своими участками (обмен участками между разными молекулами ДНК или РНК называется рекомбинацией). Рекомбинация — важнейший источник наследственной изменчивости наряду с "обычными" мутациями. В опытах с колониями РНК рекомбинация происходит сама собой, бесконтрольно, но в живой клетке она находится под контролем разнообразных и сложных регуляторных систем. Очень важно понять, что изменения наследственной информации нужны всему живому не только в геологическом масштабе времени, чтобы постепенно совершенствоваться в течение миллионов лет. Естественный отбор не может "заглянуть" так далеко, поэтому и специальные механизмы для достижения столь отдаленных целей не могут развиться. Но наследственные изменения нужны здесь и сейчас, они необходимы нам постоянно. Особенно наглядно это видно на примере простейших живых систем — вирусов. Многие ученые, правда, не считают их живыми организмами, поскольку они не могут размножаться без помощи чужих клеток, но все же многие свойства живого у них есть. Да и кто в этом мире может похвастать абсолютной самодостаточностью? Разве что "отважный странник", подземный микроб, о котором рассказано во второй главе. На примере вирусов хорошо видно, как они нарочно позволяют определенному количеству мутаций совершаться при каждой репликации. Таким способом они контролируют скорость мутирования и фактически превращают эволюцию в составную часть своего жизненного цикла, чуть ли не в основной компонент своего поведения. Вирусы-мутанты помогают друг другу в борьбе за выживание. Большинство вирусов, вызывающих болезни человека, — РНК-содержащие. Их наследственный материал хранится в форме РНК, а не ДНК, как у всех других форм жизни. Среди немногочисленных белков, закодированных в геноме таких вирусов, присутствует фермент РНК-зависимая РНК-полимераза, синтезирующий новые копии вирусной РНК (см. главу 1). Популяции РНК-содержащих вирусов неоднородны: они состоят из целого набора генетически различающихся линий. Такие полиморфные популяции называют "квазивидами" — по аналогии с видами настоящих живых организмов, которые тоже всегда полиморфны. Процесс удвоения (репликации) вирусной РНК происходит с большим числом ошибок (мутаций), благодаря чему могут быстро возникать новые варианты вируса. У полиовируса — возбудителя полиомиелита — на каждый акт репликации приходится в среднем 1,9 мутаций. При этом, конечно, появляется много нежизнеспособных вариантов, однако эти потери оправданы. Высокая скорость мутирования помогает вирусам приспосабливаться к меняющимся условиям — к деятельности иммунной системы хозяина, новым лекарствам, переходам от одного хозяина к другому и из ткани в ткань. Марко Виньюцци из Калифорнийского университета в Сан-Франциско (США) и его коллеги, изучающие полиовирусов, предположили, что дело здесь не ограничивается поиском оптимального для данной ситуации варианта генома методом "случайного попадания". Возможно, возникающие в пределах квазивида вариации могут помогать друг другу за счет разделения функций. Например, в одной линии может возникнуть мутация, повышающая скорость репликации вирусной РНК, в другой линии — другая мутация, повышающая, например, эффективность самосборки белковых молекул в вирусную оболочку — капсид. Поскольку обе линии живут и размножаются в одной и той же хозяйской клетке, они могут пользоваться "достижениями" друг друга. Эффективная РНК-полимераза первой линии будет размножать и геномы второй, а более эффективные капсидные белки второй линии будут "упаковывать" и РНК первой. Кстати, не исключено, что совместить обе эти мутации в одном и том же геноме просто невозможно. Вирусный геном очень мал, и у него не так уж много степеней свободы, то есть вариантов мутаций, совместимых с "жизнью" вируса. Бывает даже, что у двух разных генов имеется общий кусок, настолько вирусы экономны в отношении наследственного материала. В этом случае изменения в одном белке неизбежно будут приводить к изменениям в другом. Возможность экспериментальной проверки гипотезы о взаимопомощи среди вирусов появилась благодаря тому, что Виньюцци и его коллегам удалось обнаружить и выделить мутантную форму полиовируса со "сверхточной" РНК-полимеразой, совершающей очень мало ошибок при копировании РНК. Эта мутация происходит из-за замены глицина (G) серином (S) в 64-й позиции РНК-полимеразы. В соответствии с этим мутация получила название G64S. Эта мутация ведет к тому, что вирусы начинают мутировать с аномально низкой частотой — 0,3 мутации на геном вместо положенных 1,9 (Мутация G64S закрепилась у вирусов в процессе приспособления к одному из лекарств, которое делает скорость мутирования у вирусов выше допустимого предела ). Первым делом ученые проверили, действительно ли скорость мутирования важна для приспособляемости вирусов. Это подтвердилось: вирусы G64S приспосабливались к неблагоприятным условиям (лекарствам, ингибиторам) гораздо медленнее своих "диких" собратьев. Кроме того, вирусы G64S оказались неспособны проникать в спинной и головной мозг зараженных мышей, как это делают нормальные полиовирусы с высокой скоростью мутирования. Однако искусственное увеличение темпа мутагенеза привело к тому, что вирусы G64S стали проникать в мозг и размножаться там. При этом полиморфизм вирусной популяции вырос, но мутация G64S сохранилась у всех линий. Исследователи провели серию остроумных экспериментов, показывающих, что общая "эффективность" популяции вирусов зависит не от наличия в ней какой-то одной особо удачной линии, а от кооперативного взаимодействия нескольких разных линий, помогающих друг другу. Например, удалось показать, что вирусы G64S сами по себе не способны проникать в мозг, но успешно проникают туда в компании с другими вирусными популяциями — как "дикими", так и другими G64S, предварительно подвергавшимися действию искусственных стимуляторов мутагенеза. Следовательно, одни линии вирусов помогают другим преодолеть гематоэнцефалический барьер (Утолщение оболочки кровеносных сосудов мозга препятствует проникновению крупных молекул и частиц, в том числе вирусов, из крови в мозг. Аналогичным образом устроен у млекопитающих и "вейсмановский" гематотестикулярный барьер, препятствующий проникновению вирусов в семенники). Эксперименты блестяще подтвердили гипотезу о взаимовыгодной кооперации между разнообразными мутантами, составляющими вирусную популяцию — квазивид. Это означает, что эволюционирующей единицей является не отдельная линия и тем более не один вирус, а весь квазивид в целом, причем внутреннее разнообразие — залог успеха. Одна линия, даже самая совершенная, всегда будет проигрывать полиморфному квазивиду, включающему несколько взаимодополняющих линий. (Источник: Vignuzzi et al. Quasis pedes diversity determines pathogenesis through cooperative interactions in a viral population // Nature. 2006. V. 439. P. 344-348.) Частота мутаций под контролемЯрким примером того, как живые организмы регулируют скорость мутагенеза выгодным для себя образом, является имеющаяся у бактерий система "спасения утопающих" — SOS-response. Бактерия, как и любая живая клетка, не может "рассчитать", какое именно изменение генома ей в данный момент выгодно, и не может перекроить свои гены по заранее намеченному плану. Но иногда, когда условия жизни становятся невыносимыми, бывает выгодно увеличить частоту возникновения случайных мутаций во всем геноме или в отдельных его участках. И делать это бактерии умеют. Например, у кишечной палочки обнаружены так называемые SOS-гены, включающиеся в экстренных случаях. Один из них — ген dinB — кодирует склонную к ошибкам ДНК-полимеразу. В благоприятных условиях у бактерии включены гены обычных, редко ошибающихся ДНК-полимераз, и скорость мутирования остается низкой. Активизация гена dinB приводит к резкому увеличению частоты мутаций. В некоторых смертельно опасных ситуациях это может оказаться спасительным для гибнущей популяции микробов: вдруг какой-то из возникших мутантов окажется более жизнеспособным в данных условиях? Бактерии, таким образом, используют увеличение частоты мутирования как экстренную меру самосохранения. Молекулярные биологи уже научились ловко манипулировать этим свойством бактерий и активно используют его для создания различных экспериментальных генно-инженерных конструкций.
Бактерия Salmonella typhimurium Недавно шведские ученые при помощи таких конструкций сумели доказать, что у бактерий имеются эффективные средства для уменьшения вреда, приносимого накапливающимися в геноме мутациями (Sophie Maisnier-Patin, John R. Roth, Asa Fredriksson, Thomas Nystrom, Otto G. Berg, Dan I Andersson. Genomic buffering mitigates the effects of deleterious mutations in bacteria // Nature Genetics. 2005. V. 37. №12. P. 1376-1379.). Исследователи задались вопросом: как меняется жизнеспособность организма в ходе накопления в геноме случайных мутаций? Для своего эксперимента ученые создали настоящее чудо генной инженерии — бактерию с регулируемой скоростью мутагенеза. Для этого они соединили ген dinB, кодирующий склонную к ошибкам ДНК-полимеразу, с промотором, который активируется сахаром арабинозой. Промотор — это регуляторный участок ДНК, который определяет, как и когда будет работать соседний с ним ген. Получившуюся конструкцию вставили в геном бактерии Salmonella typhimurium. Это дало возможность очень тонко регулировать скорость мутагенеза генно-модифицированной бактерии, просто меняя концентрацию арабинозы в среде. Чем больше арабинозы, тем активнее работает ген dinB и тем больше ошибок-мутаций происходит при репликации (копировании) молекулы ДНК.
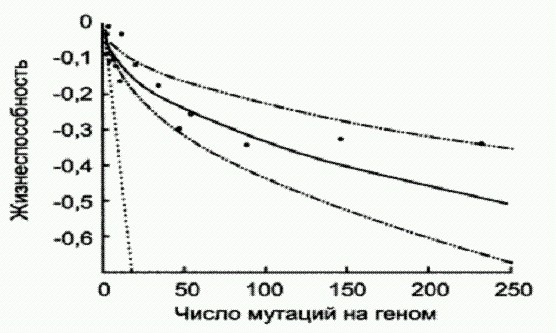
Снижение жизнеспособности (вертикальная ось) по мере роста числа мутаций сначала идет быстро, а потом замедляется (черные точки). Наклонный пунктирный отрезок показывает, каким было бы снижение жизнеспособности без эффекта "взаимной нейтрализации» Авторы показали, что мутации у модифицированной бактерии происходят более или менее случайным образом и распределяются равномерно по всему геному. Жизнеспособность бактерий-мутантов оценивалась по скорости их размножения. Оказалось, что по мере накопления мутаций жизнеспособность сначала снижается быстро, но в дальнейшем, когда число мутаций переваливает за 3-5 десятков, снижение жизнеспособности резко замедляется. Оказалось, что снижение вредоносности мутаций по мере роста их числа связано с деятельностью белков-шаперонов, обеспечивающих правильное сворачивание (укладку) белковых молекул. Повышение числа мутантных (и потому неправильно "свернутых") белков в клетке приводит к росту производства шаперонов, которым иногда удается помочь мутантному белку свернуться правильно. Таким образом, живая клетка в некоторых случаях способна не только регулировать скорость мутирования своего генома, но и эффективно справляться с вредоносным действием возникших мутаций. Наличие подобных компенсаторных механизмов дает организмам возможность без чрезмерного ущерба для себя накапливать мутации, которые могут в дальнейшем "пригодиться" естественному отбору для создания новых форм жизни. Ведь любая мутация, вредная сегодня, может оказаться полезной завтра, когда условия переменятся. Рост изменчивости в стрессовых условиях может происходить не только за счет увеличения частоты мутирования, но и из-за сбоев в работе "компенсирующих" механизмов — например, белков-шаперонов, которые до поры до времени "маскируют" значительную часть накопившихся мутаций, не дают им проявляться. Конечно, склонные к ошибкам ДНК-полимеразы лишь увеличивают частоту мутаций, не влияя на их характер, который остается случайным. И тем не менее существование такого механизма заставляет признать, что для живых организмов мутагенез вовсе не является некой не зависящей от них внешней силой, слепым "давлением энтропии", как полагали биологи еще пару десятилетий назад. Ошибка, частота возникновения которой целенаправленно регулируется, — это уже как будто и не совсем ошибка, не правда ли? Бывает и так, что разные участки генома мутируют с разной скоростью, причем у каждого участка эта скорость довольно постоянна. По-видимому, это означает, что одним генам организм "разрешает" мутировать чаще, чем другим. "Адаптивное мутирование". Это явление обнаружено у бактерий-мутантов, которые в результате мутации утратили способность использовать в пищу определенные виды сахаров. Оказалось, что если поместить этих бактерий в среду, где именно эти сахара являются единственным источником пищи, то бактерии сначала прекращают расти, а потом среди них появляются так называемые ревертанты — микробы, у которых в результате обратной мутации функция испорченного фермента восстановилась. Так вот, частота возникновения ревертантов оказалась во много раз выше, чем следовало ожидать при случайном характере мутирования. Вполне возможно, что в действительности в данном случае имеет место не направленное мутирование, а лишь некая его имитация. Согласно одной из версий, в стрессовых условиях происходит отбор микробов, у которых испорченный ген дуплицирован (присутствует в нескольких копиях). Такие микробы получают преимущество, поскольку испорченный фермент хоть и плохо, но все-таки расщепляет данный сахар. Ну а потом уже среди этих размножившихся микробов возникают ревертанты. Большое число копий испорченного гена повышает вероятность того, что хотя бы в одной из них произойдет нужная мутация. Целенаправленное создание новых геновВ некоторых случаях сомневаться в способности клетки направлять мутационный процесс на нужные гены не приходится. Особенно ярко проявляется это в работе иммунной системы позвоночных. Биологов и медиков давно интересовал вопрос, каким образом удается белым кровяным клеткам — В-лимфоцитам — производить такое огромное разнообразие антител, используемых для борьбы с различными инфекциями.
Антитела — это белки, которые умеют безошибочно узнавать определенных бактерий, вирусов, а также любые чужеродные белки (и многие углеводы) и прикрепляться к ним, что приводит к обезвреживанию самих возбудителей или выделяемых ими токсинов. По приблизительной оценке, организм человека способен производить не менее миллиона разных антител. Даже если в организм вторгается совершенно новый вирус, которого никогда раньше не было в природе, уже через несколько дней в крови можно обнаружить антитела, которые безошибочно узнают и "связывают" именно этого возбудителя и никакого другого! Организм не может запастись заранее всеми необходимыми генами антител по двум причинам. Во-первых, такое количество генов не поместится ни в каком геноме: это привело бы к непомерному росту "расходов" на содержание в каждой клетке громадного количества ДНК. Во-вторых, как бы ни был велик запас защитных генов, в любой момент может появиться новая инфекция, для борьбы с которой не подойдет ни одно из имеющихся антител.
Сейчас Арала как единого водоема уже не существует: он разделился на два изолированных, быстро пересыхающих "озера" - Большой и Малый Арал.Резкое увеличение солености привело к вымиранию большей части животных и растений. В результате внезапной перемены условий уцелевшие виды начали быстро эволюционировать. У них резко возросла изменчивость и появились целый "букеты" новых форм. самое интересное. что все эти процессы протекали очень сходным образом в двух разобщенных водоемах - Большом и Малом Арале!
Плодовые тела, образуемые бактериями Myxococcus xanthus.
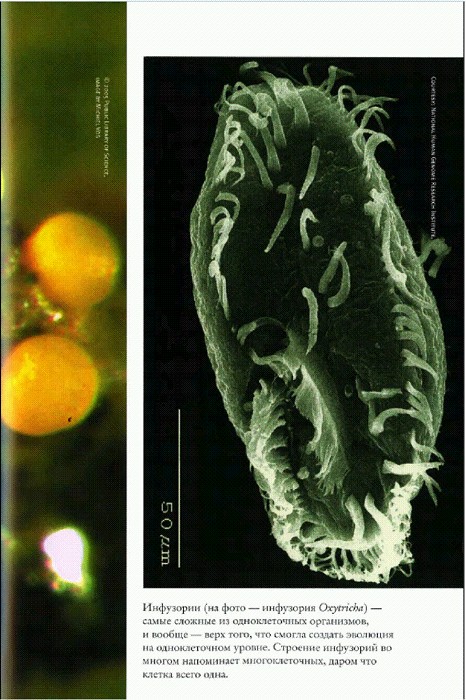
Инфузории (на фото — инфузория Oxytricha) — самые сложные из одноклеточных организмов, и вообще — верх того, что смогла создать эволюция на одноклеточном уровне. Строение инфузорий во многом напоминает многоклеточных, даром что клетка всего одна.
Реконструкция аномалокариса: сегментированное тело с "плавательными лопастями" напоминает некоторых кольчатых червей. Однако передние хватательные конечности и крупные глаза на стебельках — в точности как у членистоногих.
Мало кто из древних обитателей Земли может сравниться по своей популярности со знаменитым археоптериксом, восемь скелетов которого найдено в Германии в отложениях позднеюрского возраста. Это существо сочетает в себе признаки хищных динозавров-теропод и птиц.
Взрослые клопы Megacopta punctatissima и Megacopta cribraria, выросшие без симбионтов, отличаются мелкими размерами, бледной окраской и не могут размножаться.
Гусеницы бабочки Manduca sexta в норме имеют зеленую окраску. Ученым удалось вывести новую породу, меняющую цвет зависимости от температуры.
"Прыжки" транспозонов придают причудливую окраску кукурузным початкам. Для кодирования миллиона антител понадобилось бы четыре миллиона генов, поскольку каждое антитело состоит из четырех белковых молекул. Но ведь мы знаем, что у нас не наберется и тридцати тысяч генов. Впрочем, еще задолго до прочтения генома человека стало ясно, что гены большинства антител, образующихся в крови при различных инфекциях, не закодированы в геноме изначально, не передаются по наследству, а изготавливаются по мере необходимости из небольшого числа генов-заготовок. Это производство разделено на два этапа. Сначала, на ранних стадиях развития организма, гены антител формируются комбинаторным путем из унаследованного от родителей набора заготовок. Число наследуемых заготовок сравнительно невелико, но за счет комбинаторики из них можно собрать десятки и сотни тысяч разных генов. Специальные белки режут геномную ДНК и переставляют кусочки с место на место. Этот этап создания генов антител называется V(D)J-рекомбинацией, потому что каждый ген антитела собирается из заготовок двух (V и J) или трех (V, D, J) типов. Каждый В-лимфоцит продуцирует только один тип антител. На этом этапе неизбежно возникают "неудачные" лимфоциты, опасные для организма: они производят антитела, атакующие собственные антигены (молекулы) организма. Такие лимфоциты выбраковываются, остальные сохраняются и размножаются. Этот процесс называется клональной селекцией. В результате человек или животное получает большой набор В-лимфоцитов с антителами, способными атаковать почти любые молекулы, кроме тех, которые в норме присутствуют в данном организме. Когда в организм попадает инфекция, гены антител подвергаются более тонкой "настройке". Те лимфоциты из имеющегося набора, чьи антитела проявляют наибольшее сродство к новому чужеродному антигену, начинают вносить случайные изменения в гены своих антител, точнее, в определенные участки этих генов — так называемые вариабельные области, или V-области. Именно эти участки гена отвечают за распознавание и связывание антигена (чужеродного белка или углевода). Процесс внесения множественных изменений (мутаций) в гены защитных белков в клетках иммунной системы называется соматическим гипермутированием. На основе получающихся новых вариантов генов синтезируются антитела и проверяются на эффективность, то есть на степень сродства к новому антигену. Это продолжается до тех пор, пока не будет найден высокоэффективный вариант гена, обеспечивающий надежную защиту от нового возбудителя. Лимфоциты, производящие такое антитело, начинают усиленно размножаться. Так формируется приобретенный иммунитет. После выздоровления некоторые лимфоциты могут долго сохраняться в качестве клеток "иммунной памяти", что снижает риск повторного заболевания.
Соматическое гипермутирование — сложный и не до конца изученный процесс. Он идет под контролем специальных ферментов и имеет отчасти "закономерный", а отчасти "случайный" характер. Ключевую роль играет особый фермент — цитидин-дезаминаза, который атакует нуклеотиды Ц (цитозины) в V-области гена антитела и превращает их в урацилы (У). Как мы помним, урацил в норме входит в состав РНК, но не ДНК. Присутствие урацила в цепи ДНК служит "сигналом тревоги" для ферментов, осуществляющих репарацию — починку поврежденных участков ДНК. Эти ферменты находят урацил и начинают "исправлять ошибку". При этом они вырезают вокруг урацила довольно большой кусок ДНК (длиной до 60 нуклеотидов), а потом восстанавливают его, но делают это очень неаккуратно. В результате такой неточной починки вокруг того места, где находился урацил, возникает множество мутаций. Показано, что присутствие цитозинов абсолютно необходимо для гипермутирования и что мутации возникают на расстоянии не более 30 нуклеотидов от каждого "испорченного" ферментом цитидин-дезаминазой цитозина (чаще всего — на расстоянии 4-15 нуклеотидов). Остается неясным, почему система репарации, обычно работающая очень качественно, в данном случае под видом "ремонта" занимается "целенаправленным вредительством". Конечно, эволюционистов-теоретиков не может не волновать крамольный вопрос: что если механизм гипермутирования иногда включается не только в лимфоцитах? Таким образом, у клетки есть возможность вполне целенаправленно изменять свой собственный геном. Конечно, сделать процесс создания нужного гена по-настоящему разумным клеткам так и не удалось. Они не могут исследовать новый вирус и рассчитать, какое именно антитело в данном случае требуется. Им приходится действовать "методом оптимизированного случайного поиска". Оптимизированного — потому что имеются хорошие заготовки и клетки знают, в какие участки этих заготовок следует вносить случайные изменения. И это уже немало! Целенаправленное, сконцентрированное на строго определенных генах мутирование вовсе не является уникальной чертой лимфоцитов позвоночных животных. Многие бактерии, как выяснилось, проделывают примерно то же самое с генами своих поверхностных белков — тех самых, к которым иммунная система создает антитела. Бактерии делают это, чтобы обмануть иммунную систему, и едва ли стоит удивляться, что два старинных врага сражаются друг с другом одним и тем же оружием. Гонококки обманывают иммунную систему, внося контролируемые изменения в свой геном. По данным Всемирной организации здравоохранения, 78 миллионов человек в мире ежегодно заражаются гонореей. Гонококк {Neisseria gonorrhoeae) — облигатный паразит человека: он может жить только в человеческом организме, и в ходе эволюции микроб очень хорошо адаптировался к своей "среде обитания". Он не хуже других бактерий умеет приспосабливаться к антибиотикам (см. главу "Рождение сложности"). Однако главным врагом микроба испокон веков являются не лекарства, а наша иммунная система, и гонококк выработал мощные средства борьбы с ней, причем как оборонительные, так и наступательные. Известно, что гонококк может подавлять размножение и активность лимфоцитов (Boulton I. С., Gray-Owen S. D. Neisserial binding to CEACAM1 arrests the activation and proliferation of CD4 + T lymphocytes // Nature Immunology. 2002. V. 3. E 229-236.). Но самое зловредное свойство микроба, из-за которого люди не могут выработать против него устойчивый иммунитет, состоит в его способности быстро менять структуру своих поверхностных белков — тех самых, по которым клетки иммунной системы распознают паразита. Пока иммунная система учится распознавать и обезвреживать какой-то штамм гонококка, он меняется, и размножившиеся лимфоциты (с антителами и рецепторами, "настроенными" на поверхностные белки бактерии) оказываются не у дел. Главный поверхностный белок гонококка пилин меняется не за счет обычных "случайных мутаций" — ошибок при копировании генома, а за счет контролируемого процесса генной конверсии, то есть вполне целенаправленной замены одних участков гена другими. Собственно говоря, это тот же самый механизм, благодаря которому наши лимфоциты вырабатывают миллионы разнообразных антител и рецепторов, способных распознать практически любую заразу. Можно сказать, что гонококк борется с иммунной системой ее же оружием. Однако детали механизма генной конверсии сильно различаются в иммунной системе и у гонококка. О том, как это происходит в иммунной системе, мы уже знаем. Что же до гонококка, то в его геноме помимо активного пилинового гена существует множество его неполных копий — "псевдогенов". Некоторые их участки полностью идентичны "образцу", тогда как другие сильно отличаются. Эти копии не экспрессируются, молчат. Время от времени какой-либо участок активного гена может быть заменен соответствующим фрагментом одной из копий. В результате структура пилина меняется, и рецепторы иммунной системы перестают его узнавать. Молекулярный механизм замены одних участков генома другими у гонококка пока неизвестен, однако предложено несколько гипотетических моделей (Kline K. A. et al. Recombination, repair and replication in thepathogenic Neisseriae: the 3 R`s of molecular genetics of two human-specific bacterial pathogens // Molecular Microbiology. 2003. V 50. E 3-13. ). Все эти модели предполагают, что в каждой клетке гонококка должно присутствовать как минимум два экземпляра генома. По-видимому, участки псевдогенов одного экземпляра вставляются в активный пилиновый ген другого экземпляра. Это противоречит устоявшимся представлениям, согласно которым бактерии являются гаплоидными организмами, то есть имеют один экземпляр генома в каждой клетке. В отличие от бактерий большинство растений и животных — диплоидные организмы, у них два экземпляра генома, или двойной набор хромосом в каждой клетке. Ученые из Северо-Западного университета (Чикаго, США) не только доказали, что гонококк действительно является диплоидным организмом, но и выяснили, каким образом происходит репликация (удвоение) хромосом гонококка перед клеточным делением. Авторы проводят интересную параллель с другим микробом, у которого ранее было отмечено присутствие более одного экземпляра генома, а именно с Deinococcus radiodurans, который знаменит тем, что способен выдерживать чудовищные дозы радиации, абсолютно смертельные для любого другого живого существа. Дейнококк является тетраплоидом — в его клетках присутствует сразу четыре копии генома. "Запасные" копии нужны этому обитателю ядерных реакторов для оперативной репарации (починки) ДНК. Когда под воздействием радиации в одной из хромосом возникают мутация или разрыв, запасные хромосомы, по-видимому, используются как матрицы, с которых можно скопировать "правильные" последовательности нуклеотидов в испорченную хромосому. В обоих случаях множественность генома (полиплоидия) развилась в связи с необходимостью внесения каких-то осмысленных изменений в ДНК. (Источник: Deborah М. Tobiason, Н. Steven Seifert. The Obligate Human Pathogen, Neisseria gonorrhoeae, Is Polyploid // PLoS Biology. 2006. V. 4. Issue 6.) Контролируемая перестройка генома у инфузорийОдин из самых поразительных примеров целенаправленной перестройки генома демонстрируют инфузории. Это самые сложные из одноклеточных организмов и вообще верх того, что смогла создать эволюция на одноклеточном уровне. Строение инфузорий во многом напоминает многоклеточных, даром что клетка всего одна. Например, у многоклеточных животных различают линию генеративных клеток, геном которых обычно оберегается от всяческих изменений — ведь именно этот геном передается по наследству потомкам. Кроме того, имеется и линия соматических клеток, геном которых может меняться по мере надобности. У инфузорий тоже есть два генома — генеративный и вегетативный (соматический). Генеративный, передающийся по наследству, геном хранится в маленьком ядре (микронуклеусе), содержит кучу мобильных элементов и некодирующих участков и в целом находится в нерабочем состоянии, если не сказать — в полном хаосе. Например, многие гены в нем разорваны на куски и перемешаны. Но тем не менее это нормальный, хотя и сильно запущенный большой эукариотический геном. Кстати, число генов у инфузорий и у человека примерно одинаковое — порядка 30 тысяч. Геном микронуклеуса (МИК-геном), естественно, не работает, да он и не смог бы! Он служит только для передачи генов потомству при половом размножении. Вегетативный — соматический — рабочий геном инфузории хранится в большом ядре, так называемом макронуклеусе. Он по многим параметрам сильно отличается от других эукариотических геномов. Он состоит из множества, иногда из многих тысяч отдельных "нанохромосом". Это настоящие хромосомы, только очень маленькие, обычно содержащие всего один ген. Для каждой нанохромосомы, или МАК-хромосомы, в макронуклеусе имеется очень большое число копий. Соответственно, весь МАК-геном оказывается многократно сдублирован, то есть макронуклеус является полиплоидным, тогда как микронуклеус представляет собой диплоидное ядро. У инфузории окситрихи (Oxytricba) МАК-геном по размеру в целых 20 раз меньше МИК-генома (50 млн и 1 млрд пар нуклеотидов соответственно; для сравнения, у человека — 3,5 млрд, у бактерий — обычно до 10 млн). Такое радикальное сокращение МАК-генома при его изготовлении из МИК-генома достигается за счет выбрасывания всего "лишнего". Инфузории размножаются делением, при этом делятся оба ядра. Время от времени инфузории соединяются попарно, чтобы обменяться наследственным материалом. Этот процесс называется конъюгацией и рассматривается как особая разновидность полового процесса. Во время конъюгации микронуклеус претерпевает мейоз, то есть такое деление, в ходе которого число хромосом в поделившемся микронуклеусе сокращается вдвое. Вместо одного диплоидного микронуклеуса у каждой инфузории получается по два гаплоидных (на самом деле по четыре, но два из них тут же разрушаются). Каждая инфузория передает один из двух гаплоидных микронкулеусов своей подруге, а второй оставляет себе. Микронуклеусы затем сливаются. В результате каждая инфузория снова имеет один диплоидный микронуклеус, в котором половина хромосом — ее собственная, а половина получена от партнера. Затем инфузории разъединяются и продолжают жить как жили с той небольшой разницей, что с точки зрения генетики каждая из них теперь превратилась в свою собственную дочь. Во время конъюгации или сразу после нее макронуклеус вместе со своим геномом разрушается, а затем собирается заново. За основу берется генеративный геном микронуклеуса, но он при этом подвергается радикальной перестройке. 95% МИК-генома просто удаляется. "На выброс" идут практически все мобильные элементы и некодирующие последовательности. Остаются чистые гены, почти без примесей. Но реорганизация генома не сводится к удалению не нужных здесь и сейчас участков генома. Происходит также "распутывание" — сборка работоспособных генов из разрозненных и перепутанных обрывков. Как мы помним, многие гены в МИК-геноме разорваны на мелкие кусочки и перемешаны. В промежутках между этими кусочками могут находиться длинные некодирующие вставки. Например, в МИК-геноме ген может иметь такую структуру: 2X7X5X4X8X1X3X6 (цифрами обозначены "рабочие" фрагменты гена, буквой X — ненужные вставки различной длины). В МАК-геноме этот ген будет выглядеть так: 12345678. Откуда клетка знает, в каком порядке нужно соединять обрывки? Ответ на этот вопрос был получен лишь в конце 2007 года. Исследователи из Принстонского университета установили, что для "распутывания" генетической информации инфузории используют образцы (матрицы), представляющие собой молекулы РНК, считанные с нанохромосом макронуклеуса (МАК-хромосом) перед тем, как макронуклеус был разрушен. Чтобы это выяснить, пришлось провести множество сложных экспериментов (Mariusz Nowacki, Vikram VIijayan, Yi Zhou, Klaas Schotanus, Thomas G. Doak, Laura F. Landweber. RNA-mediated epigenetic programming of a genome-rearrangement pathway // Nature. 2008. V. 451. P. 153-158.). Для проверки гипотезы о роли РНК-матриц в сборке МАК-хромосом исследователи кормили инфузорий генно-модифицированными бактериями, производящими двухцепочечные молекулы РНК, совпадающие по последовательности нуклеотидов с фрагментом одной из МАК-хромосом. Эукариотические клетки относятся к двухцепочечным РНК с опаской, принимают их за вирусов и начинают уничтожать все РНК с такой же последовательностью нуклеотидов, в том числе и обычные, одноцепочечные. Идея состояла в том, что, проглотив бактерию, инфузория сама уничтожит одну из РНК-матриц, необходимых ей для сборки МАК-хромосом. Так и вышло. В результате после конъюгации получились инфузории, у которых соответствующий участок одной из МАК-хромосом оказался собран неправильно или вообще не собран — просто оставлен в том виде, в каком он был в МИК-хромосоме. При этом все остальные МАК-хромосомы были собраны правильно. Стало быть, РНК-матрицы действительно участвуют в программируемой перестройке генома. Но что они собой представляют — являются ли они копиями целых нанохромосом или отдельных их участков? Исследователи стали выделять и анализировать РНК из инфузорий на разных стадиях жизненного цикла. Выяснилось, что через несколько часов после конъюгации (как раз тогда, когда старый макронуклеус разрушается, а новый начинает формироваться) в клетках появляются длинные молекулы РНК, соответствующие целым МАК-хромосомам вместе с концевыми участками — теломерами. Через 30-50 часов после конъюгации эти молекулы исчезают. Таким образом, перед тем как уничтожить макронуклеус вместе с вегетативным геномом, клетка снимает "резервную копию" с каждой МАК-хромосомы. Эта копия, представляющая собой молекулу РНК, в дальнейшем используется как образец для сборки новых маленьких и аккуратных МАК-хромосом из того безобразия, которое записано в МИК-хромосомах. Следующий вопрос состоял в том, насколько точно РНК- матрицы регулируют процесс сборки МАК-хромосом и можно ли управлять этим процессом, внедряя в клетку искусственные РНК-матрицы. Исследователи синтезировали несколько молекул РНК, похожих на "настоящие" РНК-матрицы, но с измененным порядком фрагментов. Например, если для МИК-гена со структурой 2X7X5X4X8X1X3X6 правильная РНК-матрица имеет вид 12345678, то в искусственной матрице какую-нибудь пару фрагментов меняли местами: 13245678.
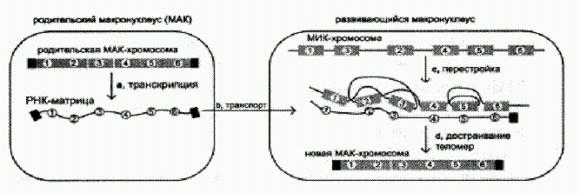
РНК-матрица, считанная с МАК-хромосомы перед разрушением макронуклеуса, служит "ключом" для распутывания генетической информации, содержащейся в МИК-хромосоме. Черным цветом обозначены концевые участки хромосом — теломеры. Впрыскивание таких матриц в инфузорий после конъюгации приводило к формированию МАК-хромосом двух типов: одни воспроизводили правильный порядок фрагментов, ведь правильные матрицы из клеток не удалялись. Другие — тот, который присутствовал в искусственных матрицах. Таким образом, РНК-матрицы осуществляют весьма точное управление процессом сборки МАК-хромосом, и при помощи искусственных матриц можно направлять этот процесс в желаемую сторону. Следующий важный вопрос — регулируют ли РНК-матрицы сборку только тех генов, которые в генеративном геноме перемешаны, то есть имеют неправильный порядок фрагментов, или же этот механизм универсален и применяется ко всем генам без исключения? Исследователи изготовили и ввели в инфузорий РНК- матрицы с неправильным порядком фрагментов для тех генов, которые в генеративном геноме не перемешаны и потому в "распутывании" не нуждаются. В итоге соответствующие гены в МАК-хромосомах оказались неправильно собраны. Значит, механизм универсален. Из этого, кстати, следует интересный эволюционный вывод. Поскольку у инфузорий уже развилась универсальная система "распутывания" измельченных и перепутанных генов, дальнейшая фрагментация МИК-генов и перестановки их частей уже не будут отсеиваться отбором. Ведь есть распутывающий механизм, ему все равно, он все исправит. Видимо, потому-то МИК-геномы инфузорий и пришли постепенно в состояние хаоса. Глядя на рисунок, можно понять, что система изначально могла развиться просто для удаления лишних кусков генома, а "распутывающая" функция ее возникла при этом автоматически, сама собой, как некий довесок — сначала ненужный, но потом ставший необходимым. Таким образом, информация о последовательности, в которой нужно сшивать обрывки генов генеративного генома, передается потомству инфузорий "неклассическим" способом — в виде молекул РНК. А ведь это не такая уж маленькая часть наследственной информации! Могут ли РНК-матрицы передавать потомству также и информацию о последовательности отдельных нуклеотидов? До сих пор речь у нас шла только о последовательности фрагментов генов, то есть о кусках длиной в десятки и сотни нуклеотидов. Каждый ген, как известно, может существовать в виде нескольких вариантов (аллелей), различающихся единичными нуклеотидными заменами или вставками. Поэтому соответствие РНК-матрицы и собираемых на ее основе МАК-хромосом далеко не всегда является абсолютным. Отдельные нуклеотиды могут различаться, и это не мешает правильной сборке. В принципе не исключено, что какие-то нуклеотидные замены могут передаваться из РНК-матрицы в собираемую МАК-хромосому. Конечно, инфузориям нет смысла переносить в МАК-хромосому все различия такого рода. Ведь тогда МАК-хромосомы после конъюгации оставались бы полностью идентичными материнским, и конъюгация потеряла бы всякий смысл. Но, как выяснилось, некоторые нуклеотидные замены все-таки переносятся в МАК-хромосомы из РНК-матриц. Это, однако, происходит не по всей длине собираемого гена, а только в непосредственной близости от мест "сшивки" фрагментов. Это очень важный факт, и он однозначно свидетельствует о том, что в сшивке кусочков ДНК у инфузорий принимает участие только что открытый механизм починки ДНК на основе РНК-матриц (см. раздел "Новые способы работы с информацией" в главе 9). Могут ли подобные системы "редактирования" генома, основанные на использовании РНК-матриц, работать и у других организмов, а не только у инфузорий? Почему бы и нет? Нужно искать. Череда открытий последних лет однозначно показывает, что живая клетка по-прежнему таит в себе множество неизвестных нам молекулярных механизмов, в том числе и таких, которые используются для целенаправленного изменения собственного генома. И так далееМы рассмотрели далеко не все известные на сегодняшний день механизмы, посредством которых живые организмы могут управлять изменениями собственных геномов или геномов своего потомства. Рассказать обо всех случаях такого рода в рамках одной небольшой книги едва ли возможно, но о некоторых из них все же необходимо вкратце упомянуть — для полноты картины.
Метилирование ДНК как средство регуляции мутагенеза. Клетка располагает множеством разнообразных средств для регуляции активности генов, и одним из них является метилирование ДНК. Метилирование — это прикрепление метильных групп (-СН3) к некоторым нуклеотидам. Мы еще вернемся к этому явлению в главе "Наследуются ли приобретенные признаки?", а сейчас хотелось бы обратить внимание только на одну особенность этого процесса. Как выяснилось, метилирование нуклеотида повышает вероятность его мутирования. Чаше всего метилируется цитозин (Ц). Метилированный цитозин с большой вероятностью может самопроизвольно превратиться в тимин (Г). Таким образом, метилированные нуклеотиды превращаются в "горячие мутационные точки". Между тем хорошо известно, что метилирование ДНК — процесс отнюдь не хаотический, он идет под управлением сложных молекулярных систем. Клетка метилирует не все нуклеотиды подряд, а лишь те, которые она "хочет" прометилировать. Что же получается? Получается, что клетка имеет возможность по собственному усмотрению размечать свой геном, расставляя на нем "горячие мутационные точки". Вот вам и случайные мутации! Природные генные инженеры. Если вы, дорогие читатели, считаете, что честь изобретения генной инженерии принадлежит человеку, то мне придется вас разочаровать. Генная инженерия была изобретена бактериями задолго до появления Homo sapiens. Мы же не только без спросу позаимствовали чужую идею, но и самих изобретателей заставили себе служить. Жертвой этого вопиющего нарушения авторских прав стал микроб Agrobacterium tumefaciens из группы альфа-протеобактерий (то есть близкий родственник предков митохондрий, о чем говорилось в главе "Великий симбиоз"). У предков агробактерии, как и у многих добропорядочных микробов, имелся особый молекулярный аппарат, предназначенный для сексуальных контактов с другими микробами. Микробный половой процесс сводится к внесению в цитоплазму других микроорганизмов фрагментов своей ДНК в ходе конъюгации (подробно об этом говорится в главе "Наследуются ли приобретенные признаки?") (Хотя половой процесс у прокариот и инфузорий называется одинаково — "конъюгация", его механизмы очень сильно различаются. В отличие от инфузорий у бактерий при конъюгации один микроб является донором, а другой — реципиентом, то есть гены передаются только в одном направлении. Кроме того, передается не весь геном, а только часть его). Хитрая агробактерия стала использовать этот полезный аппарат для того, чтобы вводить свою ДНК в клетки растений, на которых агробактерия паразитирует. В результате такой инъекции бактериальные гены начинают работать в растительной клетке, это приводит к усиленному делению клеток и образованию опухоли, в которой агробактерия чувствует себя очень комфортно. Это самая настоящая генная инженерия без всяких оговорок, то есть введение чужеродного генетического материала с целью направленного изменения свойств организма-хозяина. Вся современная генная инженерия растений основана на нещадной эксплуатации агробактерии, которую заставляют вводить в клетки растений различные фрагменты ДНК по прихоти экспериментаторов. Итак, мы видим, что от полового процесса до целенаправленного изменения наследственных свойств — один шаг. А если подумать еще немного, то можно понять, что и шага-то делать не надо. Мы уже пришли. Ведь когда одна бактерия вводит другой бактерии свои гены, разве она не меняет при этом ее наследственные свойства? И разве этот процесс не происходит в известной мере целенаправленно? И разве то, что именно и кому именно будет введено, не может повлиять на эволюцию? Или, может быть, вы думаете, что бактериям все равно, какие гены и кому вводить? Им это далеко не все равно, о чем свидетельствуют имеющиеся у прокариот сложные механизмы химической коммуникации и взаимного узнавания. Вот теперь мы подобрались вплотную к одному секрету, который на самом деле лежит на поверхности. Все живые организмы заботятся о наследственности своего потомства, и естественный отбор вполне в состоянии поддержать такие изменения, которые делают эту заботу более эффективной. Иными словами, эволюция может создавать средства оптимизации самой себя. "Приспособления для эволюции", считавшиеся запретными в классическом неодарвинизме (СТЭ), на самом деле не только возможны — они существуют и окружают нас буквально со всех сторон. Выбор брачного партнера. Я думаю, что читатели уже все поняли. Можно ли спорить с тем, что, выбирая себе брачного партнера, мы тем самым манипулируем наследственными свойствами (геномом) своего будущего потомства? Пользуясь случаем, хочу "разоблачить" и еще одну устаревшую догму — о безвыборочном или равновероятном скрещивании (панмиксии) в популяции. Впрочем, называть это представление догмой, пожалуй, не стоит: биологи никогда не воображали, будто в природных популяциях скрещивание происходит абсолютно безвыборочно. Однако отклонения от случайного скрещивания традиционно считались несущественными. На самом деле формирование брачных пар никогда не бывает случайным, всегда присутствует элемент выбора. И выбор осуществляется если не на уровне организма, то на уровне половых клеток. Процесс выбора регулируется множеством разнообразных механизмов, поражающих своей сложностью и эффективностью. Даже бактерии не меняются генами с кем попало: у них есть целый ряд способов отличить "своих" от "чужих" и выбрать из множества потенциальных партнеров оптимального. У эукариот способы и алгоритмы выбора необычайно развились и усложнились. По-видимому, многие организмы умеют на основе химических сигналов оценивать степень своего родства с потенциальным партнером. Результаты такого анализа учитываются при принятии "брачного решения". Как показали исследования последних лет, механизмы различения своих и чужих на уровне многоклеточных организмов удивительным образом связаны и переплетены с аналогичными механизмами на уровне отдельных клеток и молекул. Иммунная система, задача которой — отличать свое от чужого на молекулярном уровне, может участвовать и в оценке степени родства потенциального партнера. В обоих случаях важную роль играют белки из надсемейства иммуноглобулинов. Специальные эксперименты показали, что даже люди в состоянии извлечь ключевую информацию о генотипе другого человека по запаху его одежды. Это кажется фантастикой, но это факт. Например, показано, что женщине больше всего нравится запах тела тех мужчин, чей генотип по определенным параметрам наиболее сильно отличается от ее собственного. Рыбка колюшка в аналогичной ситуации предпочитает промежуточный вариант: не слишком генетически близкого, но и не слишком неродственного самца. А есть и такие случаи, правда, редкие, когда животные вполне целенаправленно стремятся к инбридингу — скрещиванию с ближайшими родственниками. Совершенно очевидно, что смещение брачных предпочтений в ту или иную сторону может влиять на эволюцию. Например, предпочтение "максимально неродственных" может привести к межвидовой гибридизации. Мы должны иметь в виду, что, вопреки расхожему мнению, межвидовые гибриды часто оказываются вполне жизнеспособными и плодовитыми. Напротив, предпочтение "максимально родственных" может привести к тому, что компактная группа особей, желающих скрещиваться только друг с другом, самоизолируется от остальных представителей своего вида. В результате исходный вид разделится на два, и произойдет акт видообразования (См.: http://evolbiol.ru/mate_recognition.htm). Эволюция механизмов адаптацииПроцесс приспособления, или адаптациогенез, составляет главное содержание эволюции. Он может идти на разных уровнях: строения организма, его поведения, структуры коллектива. На всех этих уровнях можно наблюдать постепенный переход от первичных, примитивных, медленных способов адаптации, основанных на случайных мутациях и отборе, к более эффективным и быстрым. Роль случайности снижается; роль закономерных, контролируемых процессов растет. Исходным, базовым алгоритмом эволюции является случайный поиск, или метод проб и ошибок. Он и сегодня остается очень важным. Однако на всех уровнях адаптациогенеза можно наблюдать постепенное развитие механизмов, сужающих рамки случайности и, таким образом, оптимизирующих этот алгоритм. Впрочем, полностью исключить элемент случайного поиска, по-видимому, невозможно не только в биологической, но даже и в социальной и культурной эволюции человека. 1. Уровень строения организма включает все биохимические, физиологические и морфологические признаки. Уже на этом уровне многие формы жизни выработали более быстрые и эффективные способы приспосабливаться, чем случайный поиск, осуществляемый по схеме "случайные мутации + отбор". В этой главе мы познакомились с некоторыми из таких способов. К механизмам оптимизации эволюционного "случайного поиска" относятся регуляция темпов мутагенеза в зависимости от условий, адаптивная конверсия генов в клетках иммунной системы и у бактерий, геномный импринтинг (о нем мы поговорим подробнее в главе "Наследуются ли приобретенные признаки). Например, при формировании нового антитела и комбинирование фрагментов ДНК, и гипермутирование — процессы, лишь отчасти случайные. Границы случайности в данном случае жестко предопределены. Комбинируются фрагменты ДНК из строго определенного ограниченного набора, гипермутирование происходит лишь в строго определенном участке гена, а отбор клонов лимфоцитов делает весь процесс однозначно направленным. В результате конечный итог подобной "последовательности случайных событий" становится строго детерминированным. Эффективное антитело против нового возбудителя непременно будет выработано — жаль только, что не всегда это происходит достаточно быстро, иначе мы никогда не умирали бы от инфекционных болезней. Такой механизм достижения цели можно назвать "оптимизированным случайным поиском". Избирательное скрещивание родительских пар представляет собой один из способов управления приспособленностью потомства (рекомбинационная изменчивость). Этот процесс контролируется сложнейшими механизмами выбора брачного партнера. Только при случайном скрещивании родители не могут воспользоваться этим способом повлиять на адаптивность потомства, но в природе безвыборочного скрещивания практически никогда не бывает. По мере роста уровня организации живых существ увеличивалась сложность и эффективность механизмов выбора брачного партнера, а значит, рекомбинационная изменчивость становилась все менее случайной. Из всего этого можно сделать очень важный вывод: эволюционируют не только организмы, виды, сообщества; эволюционируют также и механизмы эволюции. Кроме того, важнейшим способом усовершенствования адаптивных возможностей организмов является развитие адаптивных модификаций, о которых мы говорили в главе "Рождение сложности". Между прочим, приобретенный иммунитет — это яркий пример адаптивной модификации, если смотреть на дело с точки зрения целостного организма, а не с точки зрения отдельных лимфоцитов, размножающихся в нашем теле подобно каким-нибудь симбиотическим амебам. 2. На уровне индивидуального поведения четко прослеживается переход от преимущественно наследственных, генетически детерминированных стереотипов поведения к более пластичным, основанным на обучении. Точно так же, как в случае с иммунитетом выгоднее передавать потомству не жестко детерминированное средство борьбы с конкретной инфекцией, а универсальную способность к "обучению" лимфоцитов, в эволюции поведения оказалось выгоднее передавать не жестко закрепленную манеру поведения, а обучаемость. Развитие способности к обучению — крупнейшее эволюционное достижение, к которому земная жизнь шла очень долго и постепенно. Даже у одноклеточных эукариот уже есть зачаточные способности к обучению. У них обнаружены простейшие формы памяти, такие как "привыкание" и "сенсибилизация", то есть ослабление или, наоборот, обострение чувствительности к повторяющимся стимулам в зависимости от их "важности". Что уж говорить о таких высокоорганизованных животных, как муравьи или осьминоги. 3. На уровне социума идет социальный адаптациогенез. Огромное множество живых организмов — от бактерий до млекопитающих — ведут в той или иной форме общественный образ жизни. Социум как целое обладает определенными системными характеристиками, которые могут быть в большей или меньшей степени адаптивными. Здесь тоже наблюдается переход от генетически детерминированных форм социальных отношений к более гибким вариантам, при которых социум может адекватно, то есть адаптивно, реагировать на изменения среды. Например, число и размеры дочерних колоний у муравейника могут определенным "разумным", то есть адаптивным, образом меняться в зависимости от доступности ресурсов. "Есть все основания рассматривать образование отводков как механизм поддержания численности семьи на определенном, оптимальном для данного вида в данных условиях уровне", — пишет крупнейший специалист по муравьям А. А. Захаров в книге "Муравей, семья, колония" (http://evolution.powernet.ru/library/marav.htm). Многие животные и даже микроорганизмы живут поодиночке, пока условия благоприятны, а при ухудшении условий собираются вместе и формируют слаженный коллектив, что повышает шансы на выживание (см. сюжет "Способность к сложному коллективному поведению может возникнуть благодаря единственной мутации" в главе "Рождение сложности"). Однако в целом возможности такого рода у всех дочеловеческих форм жизни, включая даже высших обезьян, крайне ограниченны. Человек стал первым в истории Земли гиперсоциальным животным. Этим термином обозначают способность к практически не ограниченному, и в том числе адаптивному, изменению структуры социума. Только человек способен в зависимости от условий радикально менять структуру своих коллективов, правила взаимоотношений с сородичами, способы добычи пропитания, устройство семьи и т. д. Многие антропологи считают эту особенность чуть ли не самой главной, базовой отличительной чертой человека, которая и вывела наш вид на качественно иной уровень эволюционного развития. Получается, что появление человека разумного стало естественным и закономерным результатом общей эволюционной тенденции к росту эффективности механизмов адаптациогенеза, к оптимизации эволюционного "случайного поиска". Не потому ли человек смог стать доминирующим видом на нашей планете? Что почитать на эту тему в ИнтернетеБ. Ф. ВАНЮШИН. Материализация эпигенетики, или Небольшие изменения с большими последствиями. 2004. http://evolbiol.ru/epigeneticai.pdf М. Д. ГОЛУБОВСКИЙ. Неканонические наследственные изменения. 2001. http://vivovoco.rsl.ru/vv/journal/nature/08_01/golub.htm A. В. МАРКОВ. Обзоры на сайте "Проблемы эволюции": Эволюция на основе случайности или закономерности? http://evolbiol.ru/determinizm.htm Как отличить своих от чужих? Неканонические механизмы репродуктивной изоляции, http://evolbiol.ru/mate_recognition.htm B. А. РАТНЕР. Внешние и внутренние факторы и ограничения молекулярной эволюции. 1993. http://evolbiol.ru/ratner2.htm Г. Б. СМИРНОВ. Механизмы приобретения и потери генетической информации бактериальными геномами. 2007. http://evolbiol.ru/smirnov.htm Э. СТИЛ, Р. ЛИНДЛИ, Р. БЛАНДЭН. Что если Ламарк прав? Иммуногенетика и эволюция. 2002. http://evolbiol.ru/lamarck.htm К. X. УОДДИНГТОН. Зависит ли эволюция от случайного поиска? 1970. http://evolbiol.ru/waddington.htm R. L. CARROLL. Evolution of the capacity to evolve. 2002. http://rogov.zwz.ru/Macroevolution/carroll_2002.pdf |
|
||
|
Главная | В избранное | Наш E-MAIL | Добавить материал | Нашёл ошибку | Вверх |
||||
|
|
||||